含氟药物结构的改进
在药物分子中引入氟原子或含氟基团可改变药物分子的渗透性、代谢稳定性,调节其pKa及脂溶性,对药物分子的吸收、分布以及与生物靶点的相互作用造成影响,由此逐步成为药物筛选的一种常用手段。
2018年美国FDA批准的38种小分子药物中,18种为含氟药物,如用于治疗1型人类免疫缺陷病毒(HIV)感染的Biktarvy、治疗非转移性去势抵抗前列腺癌的Erleada(Apalutamide)。
去年,美国诺华生物医学研究所(NIBR)在ACS旗下药物化学类期刊ACS Medicinal Chemistry Letters上总结了不同结构的含氟药物在人体内可能的代谢途径,部分药物分子会分解产生氟化物及含氟的有毒代谢产物,并在某些结构的改进方面提出了可行的建议。
比如如下:
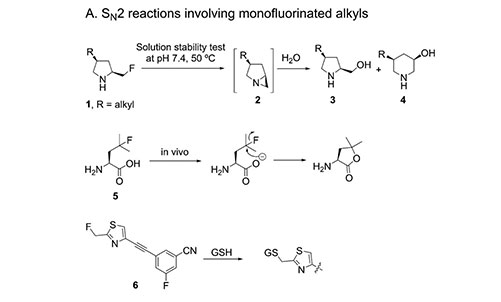
单氟烷基类药物
在分子内存在亲核性位点时,单氟烷基容易参与SN2亲核取代反应发生C-F键断裂,其在50 ℃、人体血液pH范围内可逐步分解60%-90%,释放氟负离子。相比之下,非氟母体在相同条件下分解不足2%。4-氟亮氨酸(5)中的羧酸根阴离子可亲核进攻氟取代的叔碳位点,发生C-F键断裂。该类化合物发生去氟化分解的驱动力是形成五元环内酯在热力学上更为稳定,如果将羧酸根阴离子与氟原子之间增加一个碳元便可大大降低去氟化倾向。除了分子内亲核性位点带来的影响,活泼位点(如苄位、烯丙位、羰基α位)进行单氟取代同样可与生物体内的亲核试剂发生作用,如药物分子6在大鼠脑组织匀浆中可与谷胱甘肽反应,半衰期仅为20分钟。